Dass mit der CAR-T-Zelltherapie über eine tiefe B-Zell-Depletion tatsächlich ein Reset des aberranten Immunsystems zumindest mittelfristig möglich ist, belegen die jetzt vorgestellten Daten von 15 auf median 5 (2-14) immunsuppressiven Therapien inkl. B-Zell-Depletion (n=8) und Cyclophosphamid (CYC, n=9) versagenden Patienten mit SLE (n=8, davon 7 weiblich, im Mittel 27 Jahre, medianer SLEDAI-2K 13, Biopsie-bestätigte Glomerulonephritis Grad III oder IV), idiopathischen entzündlichen Myositiden (IIM; n=3, 2 weiblich, im Mittel 42 Jahre, alle mit ILD, medianer Kreatinkinase-Spiegel 4.298 U/l) und systemischer Sklerose (SSc; n=4, 1 weiblich, im Mittel 45 Jahre, alle mit ILD, medianer mRSS 25,5). Das mediane Follow-up erstreckte sich über 15 Monate (max. 29 Monate). Die Effektivität wurde über bis zu zwei Jahre anhand der DORIS-Remissionskriterien (SLE), der ACR/EULAR-Kriterien für ein gutes klinisches Ansprechen (IIM) und dem EUSTAR-Aktivitätsindex (SSc) bewertet. Im Fokus stand zudem die Sicherheit in Bezug auf die Entwicklung eines Zytokin-Release-Syndroms (CRS), Immunzell-assoziierten Neurotoxizitätssyndroms (ICANS) oder von Infektionen.
Anhaltende medikamentenfreie Remission
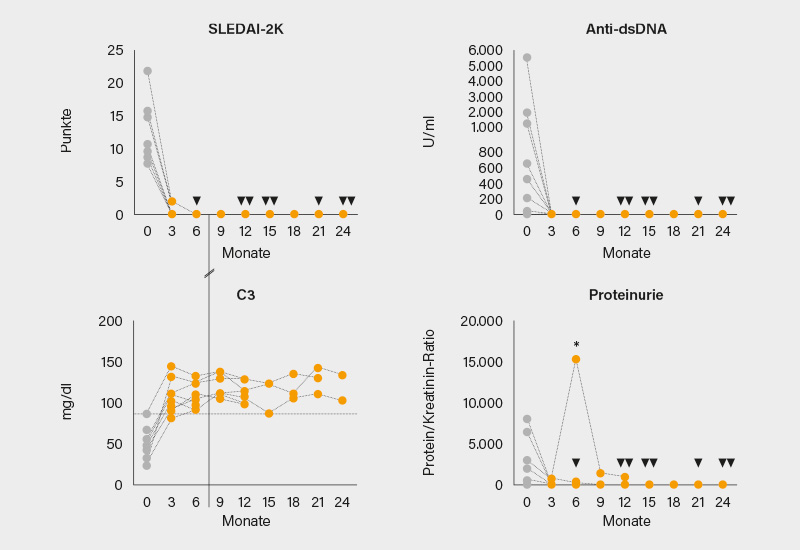
Nach T-Zell-Apherese, Aufreinigung, Virus-Transfektion mit dem CD19-Rezeptor, Expansion und Reinfusion der modifizierten CAR-T-Zellen nach Konditionierung mit Fludarabin und CYC expandierten diese in vivo bis etwa Tag 9 nach der Infusion, um dann über ca. 2-3 Monate bis zur Nachweisgrenze abzufallen. Die B-Zell-Depletion setzte innerhalb weniger Tage ein und hielt im Mittel 112 (±47) Tage an. Die Patienten blieben für durchschnittlich 15,6 Monate progressionsfrei, 100 % befinden sich in Vollremission. Alle 8 SLE-Patienten haben eine DORIS-Remission (SLEDAI 2K-Score =0), der Anti-dsDNA-Antikörperspiegel fiel auf null, der Komplement C3-Spiegel stieg an bzw. normalisierte sich und es kam zu einem drastischen Rückgang der Proteinurie (Abb.). Alle IIM-Patienten zeigen eine ACR/EULAR-Remission und alle mit SSc einen deutlichen Rückgang des EUSTAR-Aktivitätsindex-Scores. Immunsuppressive Therapien wurden bei allen Teilnehmern vor dem CAR-T-Zelltransfer komplett gestoppt und mussten bislang nicht wieder aufgenommen werden.
Zu einem CRS kam es bei 10 der Patienten (66 %), wobei dieses mit meistens Grad 1 eher schwach ausgeprägt war. Nur in einem Fall kam es zu einem CRS Grad 2 und ICANS Grad 1 (6 %), womit diese aus der Hämatologie bekannte therapieassoziierte Morbidität seltener und schwächer auftrat. Im weiteren Verlauf kam nur zu einer Pneumonie mit Hospitalisierung und einer Herpes Zoster-Infektion. Die Impftiter wurden durch die CAR-T-Zelltherapie nur moderat abgesenkt, was auf eine Persistenz langlebiger Plasmazellen hinweist.
Kompakt
Die Ergebnisse der CAR-T-Zelltherapie bei Patienten mit zuvor schweren, refraktären Verläufen sind beeindruckend, die Sicherheit bislang gut. Dennoch wird man weitere Daten zum Langzeitverlauf derart aufwändig therapierter Patienten abwarten müssen – sowohl im Hinblick auf Wirksamkeit wie auch zur Sicherheit. Vertiefende Erkenntnisse zur CAR-T-Zelltherapie werden bereits im Rahmen der in Erlangen durchgeführten CASTLE-Studie erhoben, für die derzeit weitere Patienten mit schweren Formen von SLE, SSc und IIM rekrutiert werden.
Quelle: N Engl J Med 2024; 390(8): 687-700